Cellules iPS et reprogrammation: Comment changer n'importe quelle cellule du corps en une cellule souche
La reprogrammation nous permet de transformer n’importe quelle cellule du corps en une cellule souche pluripotente. Sa découverte en 2006 a surpris de nombreux scientifiques et a changé notre vision de comment fonctionnent les cellules. La reprogrammation a ouvert des possibilités intéressantes pour l’étude et le traitement des maladies.
On pensait que les cellules souches embryonnaires étaient la source unique de cellules pluripotentes jusqu’à ce que Kazutoshi Takahashi et Shinya Yamanaka, en 2006, montrent que les cellules de la peau pouvaient être reprogrammées en cellules souches pluripotentes ‘induites’ (cellules iPS) en ajoutant artificiellement quatre gènes.
Les chercheurs furent enthousiasmés par l’opportunité qu’offraient les cellules iPS pour étudier, traiter et potentiellement guérir certaines maladies. Les cellules iPS évitent aussi plusieurs problèmes moraux liés à l’utilisation des cellules souches embryonnaires.
Ces cellules offrent aux chercheurs un excellent moyen de créer et d’étudier des cellules malades qui ont le même patrimoine génétique que celles des patients.
Les chercheurs travaillent sans relâche pour mieux comprendre comment fonctionne la reprogrammation cellulaire afin de développer de meilleures méthodes de contrôle de la différenciation cellulaire.
On utilise les cellules iPS pour rechercher et développer des traitements pour de nombreuses maladies, comme un moyen pour remplacer les cellules que les maladies ont détruites.
Les erreurs génétiques responsables de maladies varient d’un patient à l’autre. Des traitements sur mesure, utilisant les cellules iPS, pourraient corriger les défauts génétiques spécifiques d’un patient. De plus, les greffes de cellules iPS ne seraient pas rejetées par le système immunitaire du patient, puisque ces cellules sont créées à partir de ses propres cellules.
Plusieurs études montrent que les cellules iPS et les cellules souches embryonnaires fonctionnent souvent différemment, sans doute parce que les cellules iPS ne sont pas vraiment reprogrammées ‘à 100%’. Les scientifiques cherchent encore à déterminer l’incidence de ces différences sur la recherche et la médecine.
Du fait de défis techniques et de notre compréhension encore limitée des cellules iPS, il est difficile de contrôler les cellules souches et le comportement dans l’organisme des cellules obtenues à partir de cellules iPS.
Bien que des traitements médicaux à base de cellules iPS fabriquées sur mesure semblent attrayants, le développement de tels traitements efficaces et d’un coût abordable reste une tâche très difficile.
En 2006, Shinya Yamanaka a fait une découverte remarquable : il a trouvé un moyen de produire un nouveau type de cellule souche en laboratoire. Cette cellule est pluripotente – elle peut faire n'importe quelle cellule du corps – on l’appelle une cellule pluripotente induite, ou cellule iPS (de l’anglais « induced pluripotent stem cell »). Seules les cellules souches embryonnaires (ES), dérivées, chez l’homme, d’un embryon de 4-5 jours, sont naturellement pluripotentes. La découverte d’Yamanaka veut dire que toutes les cellules du corps, mis à part les spermatozoïdes et les ovules, peuvent maintenant être transformées en cellules souche pluripotentes.
Comment sont faites ces cellules iPS ? Yamanaka a ajouté quatre gènes à des cellules de la peau d’une souris. Ceci a démarré un processus à l’intérieur des cellules appelé reprogrammation et, 2 à 3 semaines plus tard, les cellules de peau ont été converties en cellules iPS. Nous pouvons maintenant faire de même avec des cellules humaines, même en ajoutant seulement 3 gènes.
Cellules souches - le futur : une introduction aux cellules iPS (vidéo sous-titrée)
Les cellules iPS et les cellules souche embryonnaires sont très similaires. Les deux peuvent donner origine à tout type de cellule, en laboratoire, dans des conditions bien contrôlées. Elles sont aussi capables de s’auto-renouveler - elles peuvent se diviser et produire des copies d’elles-mêmes indéfiniment. Elles peuvent nous aider à comprendre comment des types cellulaires spécialisés se développent à partir de cellules pluripotentes. A l’avenir, elles pourraient aussi fournir une réserve illimité de cellules et tissus de remplacement pour les patients de nombreuses maladies différentes.
En contraste avec les cellules souche embryonnaires, la production de cellules iPS n’entraine pas de destruction d’embryons. Il y a-t-il d’autres différences ? Les résultats de recherche indiquent que certains gènes des cellules iPS se comportent d’une façon légèrement différente des gènes des cellules souche embryonnaires. Les chercheurs sont en train d'étudier ceci plus en détail pour comprendre exactement quels sont les différences entre les deux types cellulaires et si ces différences sont importantes ou pas. Ceci veut dire que, en ce moment, il est trop tôt pour remplacer les cellules ES par des cellules iPS dans la recherche fondamentale.
Par la reprogrammation, les chercheurs peuvent créer des cellules iPS de patients atteints de maladies tels que la maladie de Parkinson ou la maladie d’Huntington et en suite produire des cellules spécialisées atteintes de ces maladies. Dans beaucoup de cas, il n’y a pas d’autre moyen d’obtenir ces cellules spécialisées. Il n’est pas possible, par exemple, d’étudier les cellules du cerveau d’un patient de la maladie de Parkinson, mais les scientifiques peuvent maintenant faire des cellules iPS de ces patients et les utiliser après pour produire des neurones en laboratoire. Ces cellules faites en laboratoire nous permettent de mieux connaitre la maladie et ces effets. Des modèles cellulaires de maladies comme ceci peuvent aussi servir de système d’étude pour le développent de nouveaux médicaments.
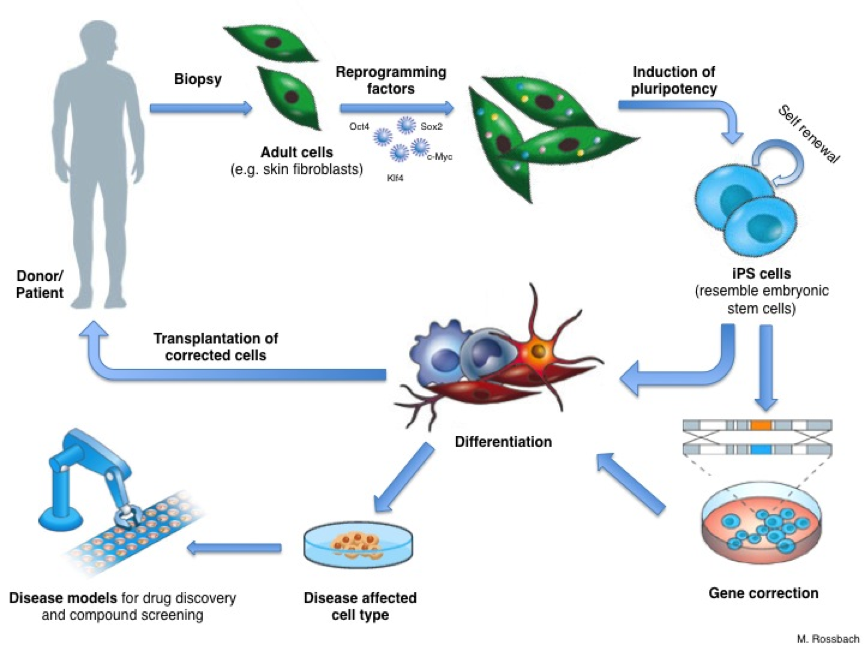
Les cellules iPS ont beaucoup de potentiel pour la médecine régénérative. En utilisant les cellules spécialisées faites à partir des cellules iPS d’un même patient pour remplacer les cellules perdues ou endommagées, il est possible d’éviter un rejet immunitaire. Dans un tel cas de thérapie de remplacement cellulaires, les nouvelles cellules données au patient seraient reconnues comme des cellules de son propre corps. Néanmoins, ceci reste théorique pour l’instant. La production de cellules iPS implique une modification génétique, ce qui peut introduire des mutations dans l’ADN provocant la formation de tumeurs. Les chercheurs travaillent pour développer des méthodes de production de cellules iPS sans modifications génétiques pour que les cellules dérivés d’iPS puissent être utilisées, sans danger, en clinique. Une possibilité est de donner des protéines ou des molécules chimiques à la place des gènes, pour démarrer le processus de reprogrammation sans avoir un effet permanent dans l’ADN de la cellule.
Cette 'fiche info' a été crée par Manal Hadenfeld et examinée par Oliver Bruestle.
Photographie de Shinya Yamanaka par Rubenstein. Images additionnels par Michael Peitz, Johannes Jungverdorben et Michael Rossbach.