Die Alzheimer-Krankheit: Wie können Stammzellen helfen?
Die Alzheimer-Krankheit ist die häufigste Ursache von Demenz. Es handelt sich um eine komplexe Erkrankung, die Nervenzellen in vielen Bereichen des Gehirns betrifft. Die wirkungsvolle Behandlung stellt deshalb eine große Herausforderung dar. Kann die Stammzellforschung dazu beitragen, diese Herausforderung in der Zukunft zu meistern?
Die Alzheimer-Krankheit ist die häufigste Ursache von Demenz. Alzheimer-Patienten leiden häufig an Gedächtnisverlust, Verwirrtheit und Stimmungsschwankungen.
Die Ursache der Alzheimer-Krankheit ist noch unbekannt; mehrere Theorien befassen sich jedoch mit zwei Proteinen, Beta-Amyloid und Tau, die in den zugrunde gehenden Bereichen des Gehirns von Alzheimer-Patienten zu finden sind.
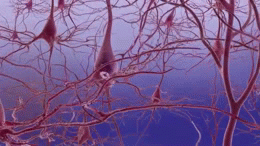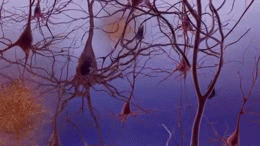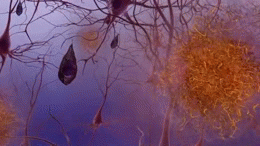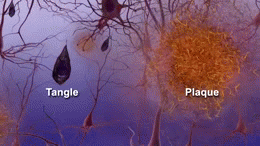
Beta-Amyloid verklumpt zu Plaques, die möglicherweise eine korrekte Signalübertragung zwischen den Nervenzellen (Neuronen) verhindern.
Tau-Proteine sind wichtig für die normale Zellfunktion. Forscher vermuten jedoch, dass zu neurofibrilläre Bündel verdrehte Tau-Proteine die Versorgung der Neuronen mit Nährstoffen stören.
Die Alzheimer-Krankheit ist gegenwärtig nicht heilbar.
Für die Alzheimer-Krankheit gibt es derzeit keine zugelassene Stammzelltherapie. Positive Effekte wurden mit der Transplantation neuralen Stammzellen in das Gehirn von Mäusen beobachtet, die eine der Alzheimer-Krankheit ähnliche Krankheit hatten. Doch die Forscher untersuchen noch, was genau diese Stammzellen tun und wie sie bei der Reparatur des Gehirns helfen könnten.
Die Forscher züchten gegenwärtig aus induzierten pluripotenten Stammzellen Neuronen, die denselben genetischen Hintergrund haben wie Menschen mit Alzheimer-Krankheit. So kann diese Krankheit genau untersucht werden. Diese Neuronen fungieren als Mittel, um nach neuen Medikamenten zur Reduzierung von Amyloid und Tau zu suchen und um Krankheitsanzeichen für eine frühere Diagnose von Alzheimer Patienten zu finden.
Im gesamten Gehirn gibt es eine Vielzahl verschiedener Nervenzellen, die bei der Alzheimer-Krankheit zerstört werden. Daher ist jeder Fall einzigartig und sehr schwierig zu behandeln.
Soll eine Stammzelltherapie erfolgreich sein, ist es unabdingbar, dass Zellen in alle geschädigten Areale im gesamten Gehirn gelangen. Es müssen auch die richtigen Arten von Nervenzellen und anderen Gehirnzellen gebildet werden sowie neue Neuronen sich korrekt mit den bereits vorhandenen Neuronen „vernetzen“. Vor allem ist es wichtig, dass diese Therapien sicher sind (also keinen Krebs oder andere Komplikationen verursachen).
Manche Forscher sind der Meinung, dass neue Neuronen, die von Stammzellen für die Alzheimerforschung erzeugt wurden, nicht genau die Eigenschaften von gealterten Gehirnzellen widerspiegeln. Andere Forscher widerrum glauben, dass diese Methode die beste ist, um die frühen Stadien der Alzheimer-Krankheit zu verstehen.
Sollte es eines Tages Stammzelltherapien gegen Alzheimer geben, beheben diese Behandlungen jedoch nicht die Ursache der Alzheimer-Krankheit. Das heißt, die Behandlungen halten möglicherweise nicht lange vor und die Betroffenen könnten Rückfälle erleiden.

Die Alzheimer-Krankheit ist die häufigste Ursache von Demenz. Zu den ersten Zeichen der Krankheit gehören häufig Gedächtnislücken oder Wortfindungsstörungen. Im weiteren Verlauf kommt es in zunehmendem Maße zu Symptomen wie Verwirrtheit, Stimmungsschwankungen und Gedächtnisverlust.
Die Ursache der Erkrankung ist noch unbekannt: Forschungen haben jedoch ergeben, dass im Gehirn von Betroffenen abnorme Ablagerungen bestimmter Proteine entstehen. Eines dieser Proteine, das so genannte Beta-Amyloid, bildet Verklumpungen, die als Plaques bezeichnet werden. Ein weiteres, das Tau-Protein, verdreht sich zu neurofibrillären Bündeln. Die Frage, ob diese Plaques und Bündel ursächlich für die Alzheimer-Symptome oder nur ein Nebenprodukt der Krankheit sind, ist nach wie vor Gegenstand der Forschung. Eine Theorie geht davon aus, dass die Plaques die Kommunikation der Nervenzellen im Gehirn behindern und die Bündel aus Tau-Protein möglicherweise die Nährstoffversorgung der Zellen stören. Die genauen Vorgänge sind noch unklar, fest steht jedoch, dass bestimmte Nervenzellen, auch als Neuronen bezeichnet, im fortgeschrittenen Stadium der Alzheimer-Krankheit verloren gehen. Aus diesem Grund wird Alzheimer den neurodegenerativen Erkrankungen zugeordnet.
Schätzungen zufolge haben bis zu etwa 1,5% der 65- bis 69-Jährigen und etwa 25 bis 30% der 90-Jährigen Alzheimer. Die genaue Ursache ist zwar nicht bekannt, aber es wird eine Reihe von Risikofaktoren mit der Krankheit in Verbindung gebracht. Der wichtigste ist ein höheres Lebensalter. Frauen haben ein höheres Erkrankungsrisiko als Männer. Erbanlagen (d. h. die familiäre Krankheitsgeschichte) spielen ebenfalls eine große Rolle. Und es werden ständig weitere Faktoren entdeckt, wie zum Beispiel eine Verbindung zu Übergewicht.
Die Alzheimer-Krankheit ist gegenwärtig nicht heilbar. Es gibt Medikamente, die einige Symptome vorübergehend bessern können, beispielsweise indem sie die Gedächtnisleistung oder die Alltagsfähigkeiten verbessern. Die meisten dieser Medikamente gehören zur Gruppe der Cholinesterasehemmer (z. B. Aricept, Exelon, Reminyl). Sie verhindern den Abbau einer im Gehirn vorkommenden Substanz namens Acetylcholin, die Signale zwischen den Nervenzellen überträgt. Es gibt jedoch keine Medikamente, die den Verlust von Nervenzellen verzögern oder aufhalten. Dank erheblicher Anstrengungen in der Forschung und Arzneimittelentwicklung konnten während der letzten zwei Jahrzehnte potenzielle neue Medikamente für den Abbau von Amyloid-Protein-Ablagerungen im Gehirn gefunden werden. Leider haben sich diese Substanzen in großen klinischen Studien nicht bewährt, was neue Fragen darüber aufwirft, wie die Erkrankung unter Laborbedingungen darzustellen und nachzuvollziehen ist. Bisher wurde überwiegend an Mäusen mit Alzheimer-ähnlichem Erkrankungsbild geforscht, so genannten Mausmodellen. Stammzellen könnten dazu beitragen, dass neue Modelle für die Krankheit zur Verfügung stehen, die eine Forschung an menschlichen Zellen ermöglichen und dass so schließlich neue Behandlungsmöglichkeiten gefunden werden.
Bislang steht keine Stammzellbehandlung für die Alzheimer-Krankheit zur Verfügung.
Die Krankheit betrifft viele verschiedene Typen von Neuronen in vielen Bereichen des Gehirns. Damit steht man vor einem komplexen Problem, wenn man darauf abzielt, das Gehirn wieder herzustellen. Obwohl die Forschung gezeigt hat, dass neurale Stammzellen (eine im Gehirn vorkommende Stammzellart) neue Neuronen erzeugen können, wäre eine Transplantation dieser Zellen in das Gehirn von Alzheimer-Patienten zur Produktion von neuen, gesunden Gehirnzellen problematisch. Eine Zulieferung von neuen Zellen an das Gehirn würde das Problem, warum Neuronen sterben, nicht lösen. Sie wären nur eine zeitweilige Hilfe, bis weitere Neuronen verloren gehen. Trotzdem könnte eine Behandlung mit neuralen Stammzellen eine große Hilfe für Patienten darstellen. Selbst wenn Personen mit Alzheimer nur eine kurze Krankheitsverzögerung erfahren, so könnte dies dennoch eine große Auswirkung auf die Lebensqualität der Patienten, die Allgemeinheit und die Wirtschaft haben. Zum Beispiel könnte eine Behandlung, die eine Verzögerung von 5 Jahren erzielt, sowohl die Anzahl der Alzheimerfälle, als auch die wirtschaftliche Belastung durch die Alzheimerkrankheit zu einem Drittel reduzieren.
Für eine Behandlung taugliche Stammzellen zu entwickeln, wird eine echte Herausforderung. Doch selbst wenn gesunde, funktionsfähige neurale Stammzellen zur Verfügung stünden und sicher transplantiert werden könnten, wäre es noch ein schwieriger Weg bis zu einem eventuellen therapeutischen Nutzen. Die Stammzellen müssten nämlich
- in die zahlreichen geschädigten Bereiche des Gehirns gelangen.
- die vielen verschiedenen Typen von Neuronen hervorbringen, die nötig sind, um die geschädigten und verloren gegangenen Zellen zu ersetzen (und zwar genau zur richtigen Anzahl, und auf keinen Fall zuviele).
- ermöglichen, dass sich die neuen Neuronen effektiv in das Gehirn integrieren, indem sie Verbindungen herstellen, um die verloren gegangenen Teile eines komplexen Netzwerks zu ersetzen.
Trotz dieser beträchtlichen Herausforderungen ist die Stammzelltransplantation an Mäusen erforscht worden und in Studien konnte ein gewisser Nutzen nachgewiesen werden. Die Forschung zu diesem Thema befindet sich in einem frühen Stadium und es sind noch viele Fragen offen. Bevor die Ergebnisse in der Entwicklung einer Therapie für den Menschen Anwendung finden, ist noch viel Forschungsarbeit notwendig.
Ein anderer möglicher Ansatz für eine Stammzelltherapie könnte die Verwendung bestimmter Arten von Stammzellen sein, um das Gehirn mit Proteinen zu versorgen, die als Neurotrophine bezeichnet werden. Im gesunden Gehirn fördern Neurotrophine das Wachstum und das Überleben von Neuronen, bei der Alzheimer-Krankheit ist die Produktion von Neurotrophinen jedoch niedrig. Neurale Stammzellen produzieren Neurotrophine und könnten daher eine Möglichkeit bieten, dieses Problem zu lösen. Um diese Theorie zu überprüfen, züchteten Wissenschaftler Mäuse mit den wesentlichen Symptomen und Merkmalen der Alzheimer-Krankheit wie beispielsweise Gedächtnisverlust. Nachdem sie neurale Stammzellen in das Gehirn der Mäuse injiziert hatten, konnten sie eine gewisse Verbesserung der Gedächtnisleistung beobachten. Derzeit wird dieser Effekt in weiteren Studien untersucht, aber der Ansatz wurde bisher nicht am Menschen geprüft.
Viele Wissenschaftler sind der Ansicht, dass Alzheimer-Patienten auf andere Weise von Stammzellen profitieren werden, bevor man potenzielle Therapien entwickelt, die auf der Transplantation von Stammzellen beruhen. Indem die Forscher Stammzellen von Alzheimer-Patienten verwenden, um im Labor große Mengen an Gehirnzellen zu züchten, können sie die Krankheit auf der Suche nach neuen Medikamenten erforschen.
Ein Tag aus dem Leben einer Demenzforscherin: Selina Wray, Wissenschaftlerin der Forschungsorganisation Alzheimer's Research UK (Video auf Englisch)
Die aktuelle Forschung verwendet einen Stammzelltyp namens induzierte pluripotente Stammzellen (iPS) für die Erforschung der Alzheimer-Krankheit. Diese Stammzellen werden im Labor hergestellt, indem man andere Zellen, die dem Patienten leicht entnommen werden können, reprogrammiert. Die so entstandenen iPS-Zellen können sämtliche Zelltypen des Körpers hervorbringen. Mit ihrer Hilfe könnte man also Zellen herstellen, die andernfalls schwer zu gewinnen sind, wie beispielsweise die im Gehirn vorkommenden Neuronen.
Wissenschaftler haben mithilfe der iPS-Technologie im Labor Neuronen gezüchtet, mit denen die Alzheimer-Krankheit erforscht wird. Die Wissenschaftler benutzen die von iPS-Zellen gezüchteten Neuronen, um Anomalien zu untersuchen, die zum Fortschreiten der Alzheimer-Krankheit beitragen könnten. Zum Beispiel untersuchen sie Unterschiede in der Art, wie Neuronen das Beta-Amyloid Protein, was zur Plaquesbildung führt, und das Tau Protein, was sich zu Bündeln verdreht, produzieren, weiterbewegen und freigeben. Die von iPS-Zellen gezüchteten Neuronen eröffnen der Wissenschaft die wertvolle Möglichkeit, an Neuronen ähnlich derer in Alzheimer-erkrankten Gehirnen in einem solchen Detail zu forschen, wie es sonst nicht möglich wäre. So können Wissenschaftler ein besseres Verständnis darüber gewinnen, wie und warum Proteinplaques im frühen Krankheitsstadium entstehen und was die Ursache für das Absterben der Neuronen ist. Auch erlaubt es den Wissenschaftlern, mit neuen Medikamenten und Therapieansätzen zu experimentieren, und gibt ihnen ein Mittel, mit dem sie nach Anzeichen suchen können, die zu einer früheren Diagnose in Alzheimer Patienten beitragen könnten, was die Chancen auf Erfolg mit neuen Behandlungen erhöht.
Einer der aktuellsten Fortschritte in der Neurowissenschaft ist die Anwendung von iPS Zellen zum Züchten von ‘Gehirnorganoiden’. Anstatt die Neuronen in einer flachen Petrischale zu züchten, läßt man Gehirnorganoide unter Bedingungen wachsen, die es neuralen Stammzellen erlauben, dreidimensionale Zellklumpen zu formen. Diese Zellklumpen beinhalten eine größere Vielfalt von Zelltypen und erschaffen dabei komplexe Zellstrukturen, die in einigen Aspekten dem menschlichen Gehirngewebe ähneln. Zum Beispiel formen Gehirnorganoide Schichten von Neuronen, genauso wie Neuronen auch im Gehirn in Schichten angelegt sind. Solche Schichten können nicht gebildet werden, wenn Zellen in flachen Schalen wachsen.
Der Vorteil von Gehirnorganoiden ist, dass sie Gehirngewebe zur Studie von Gehirnentwicklung, -funktion, -wiederherstellung und von Gehirnkrankheiten zur Verfügung stellen. Lebende Proben von menschlichem Gehirngewebe zu bekommen, ist schwierig und oft mit ethischen Problemen verbunden. Gehirnorganoide erlauben es Wissenschaftlern, Gehirngewebe für Experimente zu züchten. Ausserdem erlauben von iPS Zellen erstellte Organoide es den Wissenschaftlern, Unterschiede zwischen Gehirnzellen zu untersuchen, die unterschiedlichen genetischen Ursprungs sind, wie zum Beispiel der Vergleich von Organoiden von gesunden Individuen mit Organoiden von Alzheimer-Patienten, Wissenschaftler untersuchen alle Arten von Zellverhalten in diesen Organoiden, wie sich Zellen fortbewegen, wie sie komplexe Strukturen formen und wie sie miteinander interagieren. Zur Zeit versuchen Wissenschaftler zu ermitteln, ob Beta-Amyloid in Organoiden eher zu Plaques verklumpt als in flachen Experimentiersystemen. Falls das der Fall ist, bekämen Organoide ein außerordentlich nützliches Mittel für die Alzheimerforschung, -behandlung und zur Entdeckung neuer Medikamente.
Ein weiterer Forschungsbereich ist die Rolle, welche das Immunsystem spielt. Neueste Studien über die Gene von Alzheimer-Patienten deuten an, dass ein hyperaktives Immunsystem zu Gehirnentzündung und Schaden an Neuronen führen könnte. Wissenschaftler waren unlängst in der Lage, Mikroglia, die Immunzellen des Gehirns, von iPS Zellen von Alzheimer-Patienten zu züchten. Die Wissenschaftler wollen erfahren, wie diese Zellen mit Beta-Amyloid interagieren und ob diese Zellen möglicherweise die Alzheimerkrankheit auslösen.
Forschung mit iPS Zellen ist auch in anderen Bereichen sehr erfolgversprechend. Alzheimer ist eine Krankheit, die von Person zu Person sehr unterschiedlich sein kann. Die Alzheimerforschung an iPS Zellen, die von verschiedenen Personen stammen, tragen das Potenzial aufzudecken, warum es soviel Variation in the Alzheimerkrankheit gibt.
Manche Unternehmen mögen zwar für sich in Anspruch nehmen, Stammzelltherapien für die Alzheimer-Krankheit anbieten zu können, viele von diesen sind jedoch nicht Teil des anerkannten und sorgfältig kontrollierten Verfahrens der klinischen Prüfung. Es gibt klinische Studien der Phase I und II (d. h. Versuche zur Beurteilung der Sicherheit und der Effektivität der Behandlung) mit mesenchymalen Stammzellen für die Alzheimer-Krankheit in den USA und in anderen Ländern überall auf der Welt. Bei der Beurteilung derartiger Therapien ist Vorsicht geboten, bis die Ergebnisse dieser Studien veröffentlicht werden. Wissenschaftler haben noch ernste Fragen zur Begründung, auf denen diese Strategie basiert, und deren Sicherheit. Es muß darauf hingewiesen werden, dass Webseiten, die aktuelle klinische Studien auflisten, wie zum Beispiel clinicaltrials.gov, keine Wertung über wissenschaftliche Solidität geben und ob diese von angesehenen Institutionen geleitet werden. Es gibt derzeit keine erprobte, sichere und wirksame Stammzelltherapie für diese Krankheit in der EU oder den USA. Die Stammzelltechnologie wird jedoch bereits in Studien eingesetzt, die der intensiven Erforschung der Ursachen und Auswirkungen von Alzheimer dienen und von denen man sich wichtige Erkenntnisse über die zukünftige Entwicklung neuer Medikamente und möglicherweise auch zellbasierter Therapien verspricht.
Video: Alzheimer’s Stem Cell Research: Ask the expert – Larry Goldstein UCSD
Protein plaques and tangles explained in a ‘brain tour’ from the Alzheimer’s Association
Virtual dementia research lab from Alzheimer’s research UK
Created Out of Mind – Website dedicated to dementia awareness
Alzheimer’s Society YouTube channel
Stem cell therapies and neurological disorders of the brain: what is the truth? By Roger Barker
Dieses Informationsblatt wurde von Mahendra De Silva.
2014 überprüft und aktualisiert von Fred H. Gage, Laura Phipps, Pietro Tiraboschi, Håkan Toresson und Selina Wray.
2016 überprüft und aktualisiert von Selina Wray.
2018 von Ryan Lewis bearbeitet.
2018 überprüft und aktualisiert von Charlie Arber.
Die Übersetzung des Informationsblatts wurde durch das GermanStemCellNetwork (GSCN) im Jahr 2014 realisiert. Aktualisiert von Katrin Ottersbach.
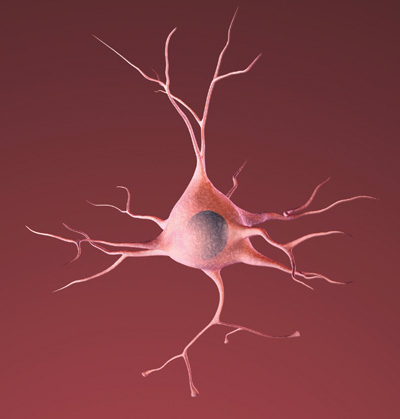
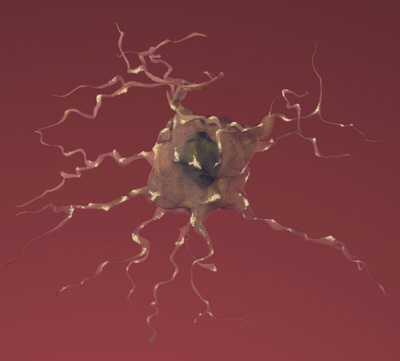
Die erste Abbildung zeigt den Verlust der Verbindungen zwischen den Neuronen im von der Alzheimer-Krankheit betroffenen Gehirn und wurde freundlicherweise vom National Institute on Aging/National Institutes of Health zur Verfügung gestellt. Die animierte Abbildung wurde von 7mike5000 aus Inside the Brain: Unraveling the Mystery of Alzheimer's Disease des National Institute on Aging erstellt. Die stark vergrößerte Abbildung der Astrozyten stammt von Nephron. Alle übrigen Abbildungen wurden freundlicherweise vom National Institute on Aging / National Institutes of Health zur Verfügung gestellt.
Die mikroskopische Aufnahme zeigt mit Fluoreszenz markierte Zellen in einem Gehirnorganoid. Gehirnorganoide erzeugen Zellschichten, die komplexe 3D-Strukturen bilden ähnlich derer im menschlichen Gehirn. Die Abbildung wurde von Charlie Arber am UCL Institute of Neurology bereitgestellt.